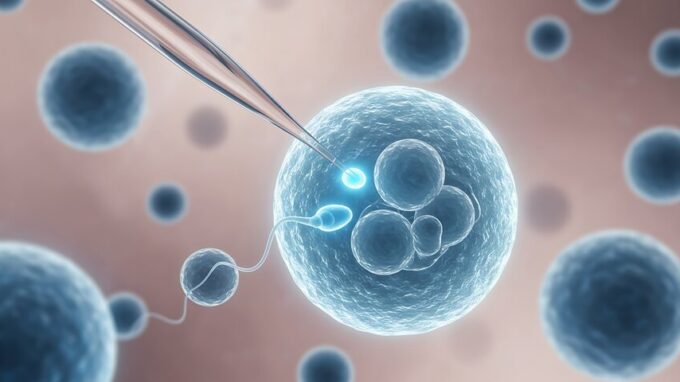
Die Herstellung von Ei- und Samenzellen aus Stammzellen zählt zu den faszinierendsten und zugleich komplexesten Entwicklungen der modernen Reproduktionsmedizin. Dieses Forschungsfeld, das eng mit der Stammzellforschung und der Reproduktionsmedizin verknüpft ist, verfolgt ein ambitioniertes Ziel: die künstliche Erzeugung funktioneller Keimzellen aus gewöhnlichen Körperzellen. Sollte dieser Ansatz erfolgreich beim Menschen umgesetzt werden, könnte er die Behandlung von Unfruchtbarkeit grundlegend verändern.
Von Körperzellen zu Keimzellvorläufern
Im Zentrum steht dabei die Technologie der sogenannten induzierten pluripotenten Stammzellen (iPS-Zellen). Hierbei werden ausgereifte Körperzellen – etwa Haut- oder Blutzellen – durch gezielte genetische Reprogrammierung in einen embryonalähnlichen Zustand zurückversetzt. Diese Zellen besitzen die Fähigkeit, sich in nahezu jeden Zelltyp zu entwickeln. Der nächste Schritt besteht darin, diese iPS-Zellen in sogenannte primordial germ cell-like cells (PGC-like cells) umzuwandeln, also Vorläuferzellen der Keimbahn. Dieser Prozess ahmt die frühe embryonale Entwicklung nach, ist jedoch im Labor nur schwer exakt zu reproduzieren, da er von einem hochkomplexen Zusammenspiel aus Signalstoffen, epigenetischen Veränderungen und Zellinteraktionen abhängt.
 Einen entscheidenden Durchbruch erzielte das Forschungsteam um Katsuhiko Hayashi in Japan. In mehreren Studien gelang es ihm und seinen Kollegen, aus Maus-Hautzellen zunächst induzierte pluripotente Stammzellen zu erzeugen und diese anschließend in Eizellen umzuwandeln. Diese künstlich hergestellten Eizellen konnten erfolgreich befruchtet werden und führten zur Geburt gesunder Mäuse. Ähnliche Fortschritte wurden auch bei der Herstellung von Spermien aus Stammzellen erzielt. Diese Experimente gelten als Meilenstein, da sie erstmals den vollständigen Entwicklungsweg von der Körperzelle bis zur funktionierenden Keimzelle im Labor demonstrierten.
Einen entscheidenden Durchbruch erzielte das Forschungsteam um Katsuhiko Hayashi in Japan. In mehreren Studien gelang es ihm und seinen Kollegen, aus Maus-Hautzellen zunächst induzierte pluripotente Stammzellen zu erzeugen und diese anschließend in Eizellen umzuwandeln. Diese künstlich hergestellten Eizellen konnten erfolgreich befruchtet werden und führten zur Geburt gesunder Mäuse. Ähnliche Fortschritte wurden auch bei der Herstellung von Spermien aus Stammzellen erzielt. Diese Experimente gelten als Meilenstein, da sie erstmals den vollständigen Entwicklungsweg von der Körperzelle bis zur funktionierenden Keimzelle im Labor demonstrierten.
Die Herausforderung der Meiose und Epigenetik
Ein zentrales Hindernis ist die korrekte Durchführung der sogenannten Meiose – ein spezieller Zellteilungsprozess, bei dem der Chromosomensatz halbiert wird und der für die Bildung von Ei- und Samenzellen essenziell ist. Fehler in diesem Prozess können zu genetischen Anomalien führen, weshalb seine kontrollierte Nachbildung im Labor eine der größten Herausforderungen darstellt. Zusätzlich müssen epigenetische Muster – also chemische Markierungen auf der DNA, die die Genaktivität steuern – korrekt „zurückgesetzt“ und neu programmiert werden, damit die künstlich erzeugten Keimzellen funktionstüchtig sind.
Trotz dieser Schwierigkeiten wurden in Tiermodellen bemerkenswerte Fortschritte erzielt. Besonders in Mausmodellen gelang es, aus iPS-Zellen zunächst Keimzellvorläufer und schließlich funktionelle Eizellen und Spermien zu generieren. Diese konnten erfolgreich zur Befruchtung eingesetzt werden und führten zur Geburt gesunder Nachkommen. Diese Ergebnisse gelten als entscheidender Beweis dafür, dass der gesamte Prozess – von der Körperzelle zur funktionierenden Keimzelle – prinzipiell möglich ist.
Neue Chancen für Betroffene
Beim Menschen steht die Forschung hingegen noch am Anfang. Zwar konnten bereits menschliche Keimzellvorläufer im Labor erzeugt werden, doch deren vollständige Reifung zu funktionsfähigen Gameten ist bislang nicht gelungen. Ein wesentlicher Grund dafür ist, dass die menschliche Keimzellentwicklung wesentlich länger dauert und komplexer reguliert ist als bei Mäusen. Zudem fehlen bislang geeignete Modelle, um die gesamte Entwicklung sicher und kontrolliert außerhalb des Körpers nachzubilden.
Das potenzielle Anwendungsspektrum dieser Technologie ist jedoch enorm. Sie könnte insbesondere Menschen helfen, die ihre Fruchtbarkeit durch medizinische Behandlungen wie Chemotherapie verloren haben, sowie Personen mit genetisch bedingter Unfruchtbarkeit. Darüber hinaus eröffnet sie theoretisch neue Möglichkeiten der Familienplanung, etwa für gleichgeschlechtliche Paare oder für Menschen, die keine eigenen funktionierenden Keimzellen besitzen.
Ethische und gesellschaftliche Fragen
Gleichzeitig wirft die Forschung an künstlichen Keimzellen eine Vielzahl komplexer ethischer, rechtlicher und gesellschaftlicher Fragen auf, die weit über die rein medizinische Anwendung hinausgehen. Ein zentraler Aspekt ist die Sicherheit der erzeugten Zellen: Da künstlich hergestellte Ei- und Samenzellen tiefgreifende genetische und epigenetische Veränderungen durchlaufen, besteht die Sorge, dass Fehler unentdeckt bleiben und an zukünftige Generationen weitergegeben werden könnten. Anders als bei vielen anderen medizinischen Eingriffen betreffen mögliche Risiken hier nicht nur die behandelte Person, sondern auch deren Nachkommen.

Ein weiterer wichtiger Punkt ist die Frage nach genetischer Integrität und Eingriffstiefe. Die Möglichkeit, Keimzellen im Labor herzustellen, könnte theoretisch auch mit genetischen Veränderungen kombiniert werden. Damit rückt die Grenze zwischen Therapie und gezielter genetischer „Optimierung“ in den Fokus – ein Thema, das eng mit Debatten über Designerbabys und genetische Selektion verknüpft ist. Auch wenn solche Anwendungen derzeit nicht im Mittelpunkt der Forschung stehen, sehen viele Ethiker hier eine potenzielle Entwicklung, die frühzeitig reguliert werden muss.
Darüber hinaus stellt sich die Frage, wer Zugang zu dieser Technologie haben wird. Hochkomplexe biomedizinische Verfahren sind oft teuer und zunächst nur begrenzt verfügbar. Es besteht die Gefahr, dass sich soziale Ungleichheiten verstärken, wenn nur bestimmte Bevölkerungsgruppen Zugang zu innovativen Fruchtbarkeitsbehandlungen erhalten. Gleichzeitig könnte die Technologie neue Möglichkeiten für bislang benachteiligte Gruppen schaffen, etwa für gleichgeschlechtliche Paare oder Menschen ohne eigene Keimzellen, was wiederum bestehende gesellschaftliche Vorstellungen von Familie verändert. Auch das Verständnis von Elternschaft und biologischer Verwandtschaft könnte sich grundlegend wandeln. Wenn Ei- und Samenzellen aus beliebigen Körperzellen erzeugt werden können, stellt sich die Frage, wie „biologische Elternschaft“ künftig definiert wird. In extremen Szenarien könnten theoretisch mehr als zwei genetische Beiträge an einem Kind beteiligt sein oder Keimzellen aus ungewöhnlichen Zellquellen stammen, was neue rechtliche und soziale Fragen aufwirft.
Nicht zuletzt spielt die regulatorische und gesellschaftliche Kontrolle eine entscheidende Rolle. Internationale Organisationen wie die International Society for Stem Cell Research arbeiten bereits an Richtlinien, um den verantwortungsvollen Umgang mit solchen Technologien sicherzustellen. Dennoch unterscheiden sich gesetzliche Rahmenbedingungen weltweit erheblich, was die Gefahr eines „Regulierungstourismus“ mit sich bringt – also der gezielten Nutzung von Ländern mit weniger strengen Vorschriften. Insgesamt zeigt sich, dass die Entwicklung künstlicher Keimzellen nicht nur eine medizinische Innovation darstellt, sondern auch grundlegende Fragen über die Zukunft der Fortpflanzung, die Definition von Familie und die Grenzen menschlicher Eingriffe in die Natur aufwirft. Eine breite gesellschaftliche Debatte sowie klare ethische Leitlinien werden daher entscheidend sein, um diese Technologie verantwortungsvoll zu nutzen.
Ausblick: Eine Technologie mit revolutionärem Potenzial
Zusammenfassend befindet sich die Entwicklung künstlicher Keimzellen an einem kritischen Übergangspunkt: Während experimentelle Studien im Tiermodell bereits beeindruckende Erfolge zeigen, steht die klinische Anwendung beim Menschen noch aus. Dennoch deutet alles darauf hin, dass dieses Forschungsfeld langfristig das Potenzial hat, die Grenzen der Fruchtbarkeit neu zu definieren und völlig neue Wege in der Reproduktionsmedizin zu eröffnen.